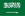1.Přímá disociace a adsorpce molekul vody
Na nenasycených kovových místech oxidů kovů nebo oxidů polovodičů (jako je Ti4+, Fe3+) se molekuly vody nejprve adsorbují v molekulární formě, následuje štěpení vazby O-H, což má za následek můstek nebo koncové hydroxylové skupiny (M-OH) a povrchové atomy vodíku. Termodynamická hnací síla tohoto procesu pochází ze silné Lewisovy kyselosti kovových iontů, díky čemuž se molekuly vody snadno disociují. Jak experimenty, tak výpočty DFT ukazují, že povrchy pokryté nízkým obsahem kyslíku mají tendenci disociovat a adsorbovat, zatímco povrchy pokryté vysokým obsahem kyslíku mají tendenci adsorbovat molekuly.
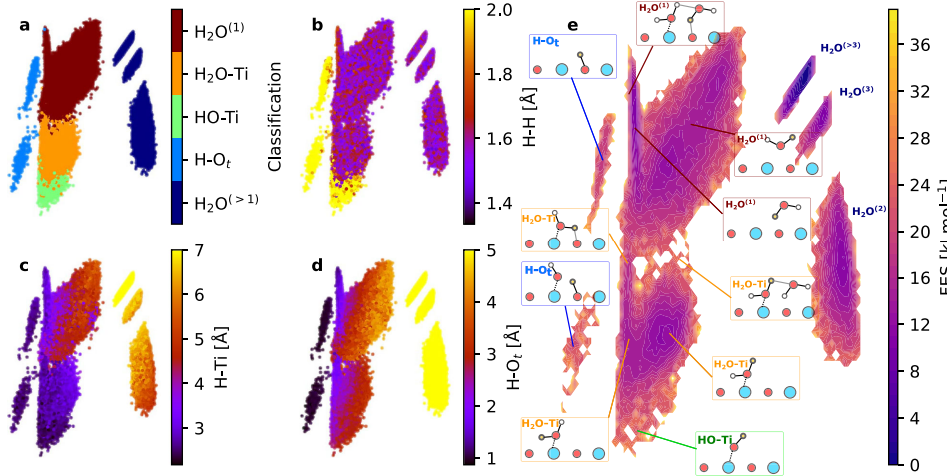
2. Generování hydroxylů zprostředkované kyslíkovou vakancí (VO).
Vakance povrchového kyslíku poskytují elektrony, díky čemuž jsou adsorbované molekuly vody náchylnější k disociaci. Poté, co se molekuly vody adsorbují na vakanci, jsou generovány dvě hydroxylové skupiny, z nichž jedna vyplňuje vakanci a druhá visí na sousedním kovu. Tento mechanismus vysvětluje jev významného zvýšení hustoty hydroxylů za redukčních nebo vysokoteplotních podmínek a úzce souvisí se změnami v koordinačním počtu kovových iontů.
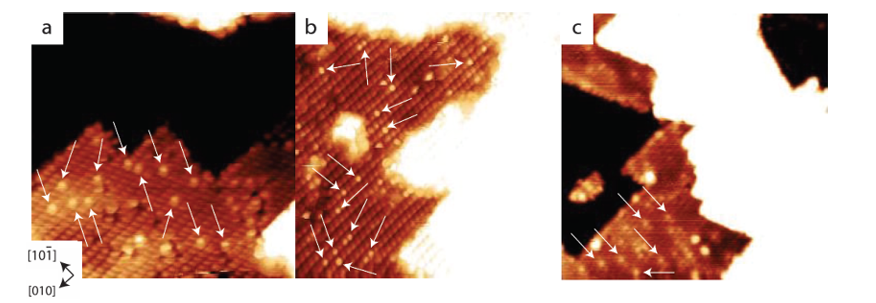
3. Přetečení atomu vodíku nebo vodíku
Na rozhraní kov/oxid H2 disociuje na kovu za vzniku H+/H⁻, který pak migruje na povrch oxidu kovu přepadem vodíku a vytváří hydroxylové skupiny s povrchovým kyslíkem. Tento proces byl přímo pozorován v katalytických systémech, jako je nízkoteplotní oxidace CO a přetečení vodíku významně zvýšilo rychlost tvorby povrchových hydroxylových skupin.
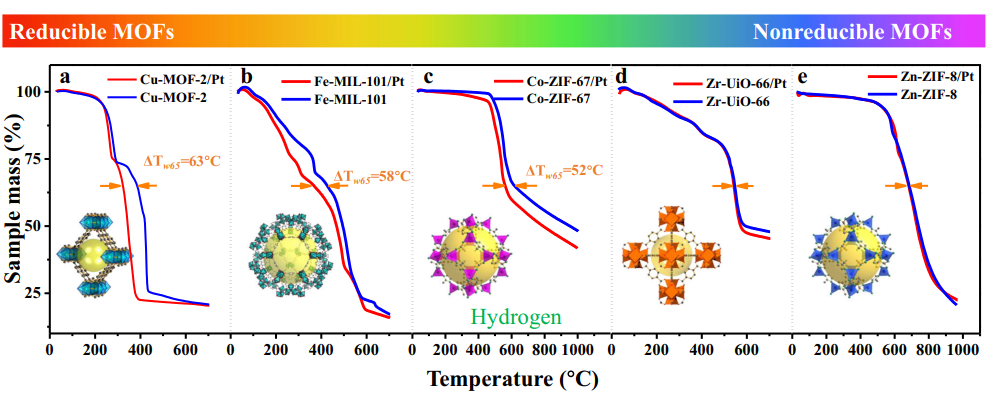
4. Fotokatalytická/UV indukovaná tvorba hydroxylů
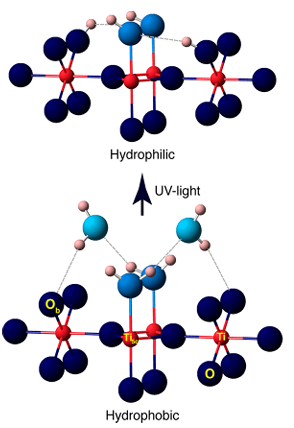
UV světlo excituje polovodiče, jako je TiO2, za vzniku párů elektronových děr, které zachycují povrchové atomy kyslíku za vzniku O ⁻, a poté reagují s adsorbovanými molekulami vody nebo hydroxylovými skupinami za vzniku povrchových OH ⁻, doprovázených produkcí hydroxylových radikálů (· OH). Experimenty ukázaly, že UV ozařování generuje další kyslíková volná místa na povrchu TiO2, které dále reagují s vodou za vzniku více hydroxylových skupin, což vede k fotoindukované superhydrofilitě.
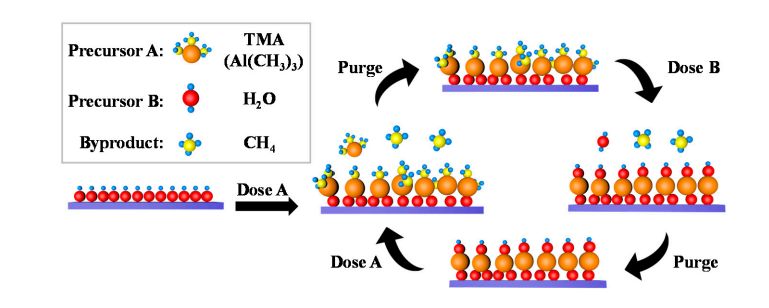
5.Tvorba hydroxylových skupin na povrchu oxidu hlinitého
Malé množství hydroxylových skupin přirozeně existuje na povrchu oxidu hlinitého a molekuly vody disociují a adsorbují se na těchto hydroxylových skupinách, čímž vzniká nový Al-OH. Během depozice atomové vrstvy (ALD) prochází TMA (trimethylaluminium) koordinační výměnou s povrchovými hydroxylovými skupinami za vzniku vazeb Al-O-Al a uvolnění metanu; Následně vodní pulz opět reaguje s vazbami Al-O k regeneraci povrchových hydroxylových skupin, čímž se dosáhne cyklické regenerace hydroxylových skupin.
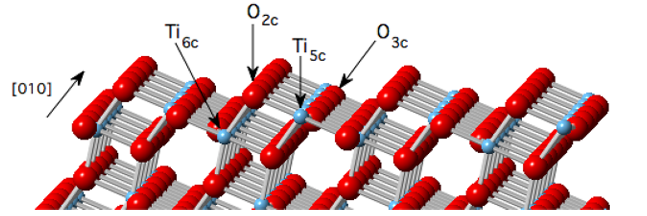
6. Rekonstrukce povrchu - Migrace kovů vede k agregaci hydroxylů
Na povrchu krystalu oxidu hlinitého nebo oxidu titaničitého migrují místní kovové ionty (jako je Al3+) do povrchových volných míst pod vysokou teplotou nebo vysokým hydrochemickým potenciálem a tvoří hydroxylové shluky typu Al (OH) 3 nebo Ti (OH) 3. Tato rekonstrukce je doprovázena deformací mřížky, která činí adsorpci hydroxylových skupin na sousedních molekulách vody příznivější a tvoří hydroxylovou základní vrstvu s vysokou hustotou.
7. Mechanismus hydrolýzy hydroxylových skupin na povrchu křemíku
Na můstkové vazbě Si-O-Si se molekuly vody spojují s křemíkovou kyslíkovou vazbou prostřednictvím synergického přenosu protonů a elektronů a vytvářejí skupiny Si-OH. Tento proces je zvláště důležitý při korozi pod napětím na špičce trhliny a povrchové hydrolýze skla a zvýšení vibrací Si-OH v tahu bylo přímo pozorováno experimentální infračervenou spektroskopií.
SAT NANO je nejlepším dodavatelem nano prášku a mikročástic v Číně, můžeme nabídnout prášek z uhlíkových nanotrubiček, jako např.
MWCNT-COOH,
MWCNT-OH, pokud máte jakýkoli dotaz, neváhejte nás kontaktovat na adrese sales03@satnano.com